Publicado em: 28/12/2017 | Edição: 248 | Seção: 1 | Página: 2-59
Órgão: Diretoria Colegiada
RESOLUÇÃO - RDC Nº 197, DE 26 DE DEZEMBRO DE 2017
Dispõe sobre os requisitos mínimos para o funcionamento dos serviços de vacinação humana.
A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso da atribuição que lhe conferem o art. 15, III e IV aliado ao art. 7º, III, e IV, da Lei nº 9.782, de 26 de janeiro de 1999, o art. 53, V, §§ 1º e 3º do Regimento Interno aprovado nos termos do Anexo I da Resolução da Diretoria Colegiada - RDC n° 61, de 3 de fevereiro de 2016, resolve adotar a seguinte Resolução da Diretoria Colegiada, conforme deliberado em reunião realizada em 12 dezembro de 2017, e eu, Diretor-Presidente, determino a sua publicação.
CAPÍTULO I
Das disposições iniciais
Seção I
Do objetivo
Art. 1º Esta Resolução da Diretoria Colegiada (RDC) tem por objetivo estabelecer os requisitos mínimos para o funcionamento dos serviços que realizam a atividade de vacinação humana.
Seção II
Da abrangência
Art. 2º Esta Resolução se aplica a todos os serviços que realizam a atividade de vacinação no país, sejam eles públicos, privados, filantrópicos, civis ou militares.
Seção III
Das definições
Art. 3º Para efeito desta Resolução são adotadas as seguintes definições:
I- alvará de licenciamento ou equivalente: documento emitido pelo órgão sanitário competente dos Estados, Distrito Federal ou dos Municípios, contendo permissão para a prestação do serviço sob regime de vigilância sanitária;
II- ambiente: espaço fisicamente determinado e especializado para o desenvolvimento de determinada(s) atividade(s), caracterizado por dimensões e instalações diferenciadas, podendo constituir-se de uma sala ou de uma área;
III- área: ambiente aberto, sem paredes em uma ou mais de uma das faces;
IV- campanha de Vacinação Pública: constitui estratégia de vacinação de um determinado número de pessoas em curto espaço de tempo, com o objetivo do controle de uma doença de forma intensiva ou a ampliação das coberturas vacinais para complementação do trabalho da rotina, promovida por órgãos públicos de saúde;
V- Certificado Internacional de Vacinação ou Profilaxia (CIVP): documento reconhecido internacionalmente, que comprova a realização de vacinação ou profilaxia.
VI- erro de Vacinação: qualquer evento evitável que pode levar ao uso inapropriado de vacinas ou causar dano a um paciente. Pode estar relacionado à prática profissional e procedimentos, com possibilidade de acontecer se as normas e técnicas não forem cumpridas;
VII- Evento Adverso Pós-Vacinação (EAPV): Qualquer ocorrência após à aplicação da vacina e que, não necessariamente, possui uma relação causal com o produto;
VIII- profissional legalmente habilitado: profissional com formação superior ou técnica com suas competências atribuídas por lei;
IX- responsável Legal ou Representante Legal: Pessoa física investida de poderes legais para praticar atos em nome da pessoa jurídica;
X- responsável Técnico (RT): Profissional legalmente habilitado, formalmente designado pelo Responsável Legal para manter as rotinas e os procedimentos de um serviço;
XI- sala de Vacinação: ambiente envolto por paredes em todo seu perímetro e pelo menos uma porta, destinada à administração das vacinas;
XII- vacinação Extramuros de Serviços Privados: atividade vinculada a um serviço de vacinação licenciado, que ocorre de forma esporádica, isto é, através de sazonalidade ou programa de saúde ocupacional, praticada fora do estabelecimento, destinada a uma população específica em um ambiente determinado e autorizada pelos órgãos sanitários competentes das secretarias estaduais ou municipais de saúde;
XIII- vacinas: medicamentos imunobiológicos que contêm uma ou mais substâncias antigênicas que, quando inoculadas, são capazes de induzir imunidade específica ativa, a fim de proteger contra, reduzir a severidade ou combater a(s) doença(s) causada(s) pelo agente que originou o(s) antígeno(s).
CAPÍTULO II
Dos requisitos para o funcionamento do serviço de vacinação
Seção I
Das condições organizacionais
Art. 4º O estabelecimento que realiza o serviço de vacinação deve estar devidamente licenciado para esta atividade pela autoridade sanitária competente.
Art. 5º O estabelecimento que realiza serviço de vacinação deve estar inscrito e manter seus dados atualizados no Cadastro Nacional de Estabelecimentos de Saúde - CNES.
Art. 6º O estabelecimento que realiza serviço de vacinação deve afixar, em local visível ao usuário, o Calendário Nacional de Vacinação do SUS, com a indicação das vacinas disponibilizadas neste calendário.
Seção II
Dos recursos humanos
Art. 7º O estabelecimento que realiza o serviço de vacinação deve ter um Responsável Técnico e um substituto.
Art. 8º O serviço de vacinação deve contar com profissional legalmente habilitado para desenvolver as atividades de vacinação durante todo o período em que o serviço for oferecido.
Art. 9º Os profissionais envolvidos nos processos de vacinação devem ser periodicamente capacitados pelo serviço nos seguintes temas relacionados à vacina:
I- conceitos básicos de vacinação;
II- conservação, armazenamento e transporte;
III- preparo e administração segura;
IV- gerenciamento de resíduos;
V- registros relacionados à vacinação;
VI- processo para investigação e notificação de eventos adversos pós-vacinação e erros de vacinação;
VII- Calendário Nacional de Vacinação do SUS vigente;
VIII- a higienização das mãos; e
IX- conduta a ser adotada frente às possíveis intercorrências relacionadas à vacinação.
Parágrafo único. As capacitações devem ser registradas contendo data, horário, carga horária, conteúdo ministrado, nome e a formação ou capacitação profissional do instrutor e dos profissionais envolvidos nos processos de vacinação.
Seção III
Da infraestrutura
Art. 10 O estabelecimento que realiza o serviço de vacinação deve dispor de instalações físicas adequadas para as atividades de vacinação de acordo com a Resolução da Diretoria Colegiada - RDC n° 50, de 21 de fevereiro de 2002, ou regulamentação que venha a substituí-la, e devendo ser dotado, no mínimo, dos seguintes itens obrigatórios:
I- área de recepção dimensionada de acordo com a demanda e separada da sala de vacinação;
II- sanitário; e
III- sala de vacinação, que deve conter, no mínimo:
a) pia de lavagem;
b) bancada;
c) mesa;
d) cadeira;
e) caixa térmica de fácil higienização;
f) equipamento de refrigeração exclusivo para guarda e conservação de vacinas, com termômetro de momento com máxima e mínima;
g) local para a guarda dos materiais para administração das vacinas;
h) recipientes para descarte de materiais perfurocortantes e de resíduos biológicos;
i) maca; e
j) termômetro de momento, com máxima e mínima, com cabos extensores para as caixas térmicas.
§ 1º Em situações de urgência, emergência e em caso de necessidade, a aplicação de vacinas pode ser realizada no ponto de assistência ao paciente.
§ 2º O equipamento de refrigeração para guarda e conservação de vacinas deve estar regularizado perante a Anvisa.
Seção IV
Do gerenciamento de tecnologias e dos processos
Art. 11 O serviço de vacinação deve realizar o gerenciamento de suas tecnologias e processos conforme as atividades desenvolvidas e que contemple, minimamente:
I- meios eficazes para o armazenamento das vacinas, garantindo sua conservação, eficácia e segurança, mesmo diante de falha no fornecimento de energia elétrica;
II- registro diário da temperatura máxima e da temperatura mínima dos equipamentos destinados à conservação das vacinas, utilizando-se de instrumentos devidamente calibrados que possibilitem monitoramento contínuo da temperatura;
III- utilização somente de vacinas registradas ou autorizadas pela Anvisa; e
IV- demais requisitos da gestão de tecnologias e processos conforme normas sanitárias aplicáveis aos serviços de saúde.
Art. 12 O serviço de vacinação deve adotar procedimentos para preservar a qualidade e a integridade das vacinas quando houver necessidade de transportá-las.
§ 1º As vacinas deverão ser transportadas em caixas térmicas que mantenham as condições de conservação indicadas pelo fabricante.
§ 2º A temperatura ao longo de todo o transporte deve ser monitorada com o registro das temperaturas mínima e máxima.
Art. 13 Os serviços de vacinação devem garantir atendimento imediato às possíveis intercorrências relacionadas à vacinação.
Parágrafo único. O serviço de vacinação deve garantir o encaminhamento ao serviço de maior complexidade para a continuidade da atenção, caso necessário.
Art. 14 A administração de vacinas em estabelecimentos privados e que não estejam contempladas no Calendário Nacional de Vacinação do SUS somente serão realizadas mediante prescrição médica.
Parágrafo único. A dispensação deve necessariamente estar vinculada a administração da vacina.
Seção V
Dos Registros e Notificações das Vacinações
Art. 15 Compete aos serviços de vacinação:
I- registrar as informações referentes às vacinas aplicadas no cartão de vacinação e no sistema de informação definido pelo Ministério da Saúde;
II- manter prontuário individual, com registro de todas as vacinas aplicadas, acessível aos usuários e autoridades sanitárias;
III- manter no serviço, acessíveis à autoridade sanitária, documentos que comprovem a origem das vacinas utilizadas;
IV- notificar a ocorrência de eventos adversos pós-vacinação (EAPV) conforme determinações do Ministério da Saúde;
V- notificar a ocorrência de erros de vacinação no sistema de notificação da Anvisa; e
VI- investigar incidentes e falhas em seus processos que podem ter contribuído para a ocorrência de erros de vacinação.
Art. 16 - No cartão de vacinação deverão constar, de forma legível, no mínimo as seguintes informações:
I- dados do vacinado (nome completo, documento de identificação, data de nascimento);
II- nome da vacina;
III- dose aplicada;
IV- data da vacinação;
V- número do lote da vacina;
VI- nome do fabricante;
VII- identificação do estabelecimento;
VIII- identificação do vacinador; e
IX- data da próxima dose, quando aplicável.
Seção VI
Da realização de Vacinação Extramuros por Serviços Privados
Art. 17 Os serviços de vacinação privados podem realizar vacinação extramuros mediante autorização da autoridade sanitária competente.
§ 1º A atividade de vacinação extramuros deve observar todas as diretrizes desta Resolução relacionadas aos recursos humanos, ao gerenciamento de tecnologias e processos, e aos registros e notificações.
§ 2º A atividade de vacinação extramuros deve ser realizada somente por estabelecimento de vacinação licenciado.
Seção VI
Da Emissão de Certificado Internacional de Vacinação ou Profilaxia (CIVP)
Art 18 O serviço de vacinação poderá emitir o CIVP.
Parágrafo único. O serviço de vacinação deverá ser credenciado pela Anvisa para a emissão do CIVP.
Art. 19 A emissão do CIVP deverá seguir os padrões definidos pela ANVISA.
§ 1º A emissão do CIVP deverá ser realizada de forma gratuita.
§ 2º A emissão do CIVP deverá ser registrada em sistema de informação estabelecido pela ANVISA.
CAPÍTULO III
Das Disposições Finais ou Transitórias
Art. 20 As vacinações realizadas pelos serviços de vacinação serão consideradas válidas para fins legais em todo o território nacional.
Art. 21 O descumprimento das disposições contidas nesta resolução e no regulamento por ela aprovado constitui infração sanitária, nos termos da Lei nº. 6.437, de 20 de agosto de 1977, sem prejuízo das responsabilidades civil, administrativa e penal cabíveis.
Art. 22 Os serviços de vacinação que se encontram, no momento da publicação desta Resolução da Diretoria Colegiada, com licença vigente para esta atividade terão o prazo de 06 (seis) meses, contados a partir da data de publicação desta Resolução, para promover as adequações necessárias para o cumprimento dos requisitos estabelecidos nesta norma.
Parágrafo único. O prazo para adequação ao requisito disposto no § 2º, art. 10 será de 02 (dois anos), contados a partir da data de publicação desta Resolução.
Art. 23 Esta Resolução da Diretoria Colegiada entra em vigor na data de sua publicação.
JARBAS BARBOSA DA SILVA JR.



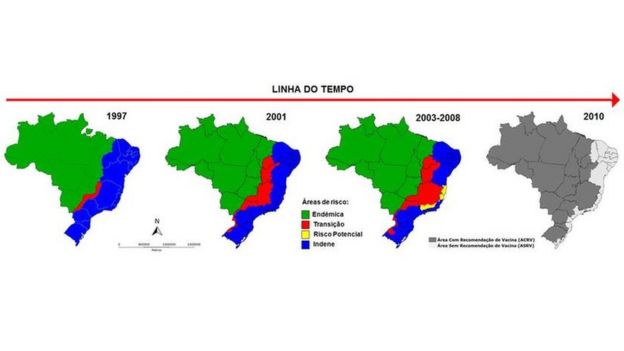 Image captionFonte: Ministério da Saúde
Image captionFonte: Ministério da Saúde